Лучевые методы диагностики остеопороза
Р. Е. Чечурин, М. П. Рубин. Москва. Городская клиническая больница №23
По оценке Всемирной организации здравоохранения проблема остеопороза по социально-экономической и медицинской значимости занимает четвёртое место вслед за сердечно-сосудистыми, онкологическими заболеваниями и сахарным диабетом. В настоящее время в диагностике остеопороза ведущее место занимают инструментальные лучевые исследования.
Анализ факторов риска а при опросе и осмотре помогает принять решение о проведении дополнительных исследований, но не позволяет поставить диагноз – не случайно остеопороз известен как «безмолвная эпидемия», редко дающая о себе знать до развития переломов. Подавляющее большинство лучевых методов используют рентгеновское излучение (при этом доминируют количественные методики) или ультразвуковые волны (количественное ультразвуковое исследование, КУИ). Оба метода распространены достаточно широко.
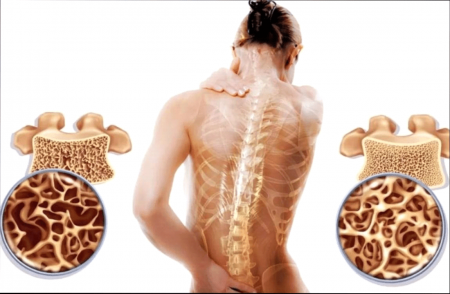
Остеопороз определяют как системное заболевание скелета, характеризующееся снижением костной массы и микронарушениями в архитектонике костной ткани, которые приводят к значительному увеличению хрупкости костей и возможности их переломов [16].
Это комплексная характеристика, описывающая состояние не только массы кости, но и её микроструктуры. По мнению ряда исследователей, основным изменением при остеопорозе является снижение общей костной прочности [18]. Это важный постулат, поскольку главной опасностью остеопороза являются переломы. Костная прочность определяется совокупностью нескольких факторов. В исследованиях in vitro показано, что 70 –80% её вариабельности определяется истинной плотностью костной ткани [6], которую сегодня измерить in vivo невозможно. Существуют различные способы косвенной оценки костной плотности, ведущим методом исследования является рентгенологический.
РЕНТГЕНОЛОГИЧЕСКИЙ МЕТОД
Традиционное рентгенологическое исследование не является средством ранней диагностики остеопороза, так как визуально снижение костной плотности можно определить при её снижении не менее чем на 25 – 30 %. Тем не менее это исследование остаётся незаменимым с клинической точки зрения, поскольку им часто приходится пользоваться для дифференциального диагноза.
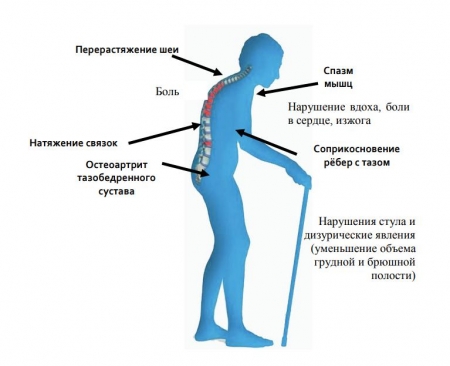
Кроме того, возможно исследование многих участков скелета; особенно важной является рентгенография грудных позвонков, снижение плотности которых часто начинается раньше, чем в других позвонках. Наконец, немаловажное преимущество традиционной рентгенографии – её доступность в практических условиях. Рентгеновская морфометрия позвоночника имеет ценность в распознавании и дифференциальной диагностике характерных для остеопороза деформаций тел позвонков. При анализе боковых спондилограмм грудного и поясничного отделов измеряют передние, средние и задние размеры (высоту) тел позвонков, вычисляют соотношения этих величин между собой и с размером заднего отдела позвонка в норме. Хотя деформации позвонков обычно означают наличие выраженного остеопороза, высказывается мнение, что возможна и достаточно ранняя диагностика этого заболевания по минимальным деформационным изменениям [2]. Радиограмметрия используется в основном в исследовательских целях.
Оцениваются рентгенограммы трубчатых костей – чаще пястных, иногда лучевой. Оценивается ширина кортикального слоя, рассчитывается кортикальный индекс (ширина кортикального слоя, делённая на диаметр кости). Этот метод не чувствителен к изменению состояния трабекулярных структур [19].
Рентгеновская денситометрия.
С практической точки зрения, большинство исследователей придерживается мнения, что измерение костной массы является наилучшим подходом к выявлению лиц, страдающих и склонных к развитию остеопороза [36]. Рентгенологический метод как способ изучения строения и функции кости при патологических процессах лучше других позволяет качественно и количественно оценить изменения, проявляющиеся уменьшением количества костного вещества. Абсорбция рентгеновских лучей костью зависит от энергии квантов, массы вещества и его плотности. Основное значение при исследовании костей имеет количество соединений кальция, имеющего сравнительно высокий атомный номер.
Для количественной оценки плотности костной ткани используются приборы, измеряющие уровень поглощения рентгеновских лучей костным веществом (костная денситометрия). Установлена связь между величиной поглощения энергии ионизирующего излучения и плотностью ткани. В единице минерализованного костного объёма содержание кальция является постоянным [27, 29], и поэтому при полной минерализации кости современные денситометры позволяют оценивать массу костей скелета.
В специально разработанных денситометрических методиках определяется проекционная минеральная плотность (в г/см2). Содержание минеральных веществ в кости связано с её прочностью сильнее других параметров. Его вклад в прочность in vitro составляет 70 – 80 % [39]. Некоторые исследователи, однако, полагают, что прочность кости не зависит от количества минеральных солей, содержащихся в ней, а определяется состоянием белковой матрицы, старением белка [7].
Денситометрические методики не лишены недостатков. Во-первых, известно, что остеопороз является заболеванием белкового матрикса кости, а содержание минералов изменяется вторично. Во-вторых, эти методики определяют лишь проекционную минеральную плотность и, таким образом, точность существенно зависит от толщины кости. Кроме того, костная ткань неоднородна, увеличение с возрастом содержания жира в костном мозгу снижает коэффициент поглощения в области измерения и, следовательно, показатель МПКТ, что, в свою очередь, ведёт к ухудшению точности [3].
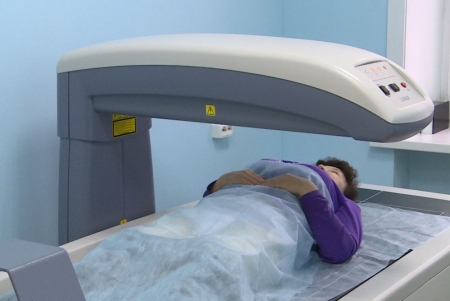
Двухэнергетическая рентгеновская абсорбциометрия позволяет исследовать несколько областей осевого и периферического скелета (наиболее информативны поясничный отдел позвоночника и проксимальный отдел бедренной кости). Рентгеновские лучи двух энергий делают возможным исследование и периферического, и осевого скелета, поскольку на плотность окружающих мягких тканей программным обеспечением делается соответствующая поправка.
Методика двухэнергетической рентгеновской абсорбциометрии признана «золотым стандартом» в диагностике остеопороза [9], поскольку она сочетает в себе ряд выгодных качеств: возможность исследования осевого скелета, хорошая чувствительность и специфичность, высокая точность и низкая ошибка воспроизводимости, низкая доза облучения (менее 0,03 мЗв), относительная дешевизна, быстрота исследования. При латеральном сканировании позвоночника возможен автоматизированный морфометрический анализ позвонков для выявления деформационных изменений. Одноэнергетическая рентгеновская абсорбциометрия, использующая лучи одной энергии, делает возможным исследование только периферических костей, окружённых минимальным количеством мягких тканей.
Радиографическая абсорбциометрия – одна из наиболее старых методик диагностики остеопороза. После обычной рентгенографии фаланг пальцев и алюминиевой пластины, используемой для сравнения оптической плотности, микроденситометр проводит сканирование рентгенограммы, при этом оценивается минеральная плотность средних фаланг [24]. Методика достаточно доступна и дёшева, тем не менее сегодня она утратила своё значение, так как состояние фаланг пальцев не позволяет, как правило, судить о наличии изменений в наиболее подверженных остеопоротическим переломам участках скелета.
Компьютерная томография позволяет получать трёхмерные изображения костной структуры и определять границы слоёв костной ткани [20]. Наибольшее распространение в диагностике остеопороза получила количественная компьютерная томография, которая представляет собой особый вид сканирования. Возможно исследование любой части скелета, наиболее часто проводят сканирование позвоночника [11]. Имеются сообщения об исследованиях бедренной кости [28]. Используется специальный калибровочный фантом; вследствие трёхмерного характера методики определяется объёмная минеральная плотность (в мг/см3) – отдельно трабекулярного и кортикального вещества [1]. Недостатками являются низкая точность, значительное облучение, высокая стоимость. Периферическая количественная компьютерная томография была разработана специально для диагностики остеопороза, позволяет отдельное исследование кортикального и трабекулярного вещества [41]. Рассчитываются показатели костной минеральной плотности (общей и трабекулярной), площадь кортикального и трабекулярного слоёв, эндостальный и периостальный периметры [23]. Как правило, исследуются лучевая или малоберцовая кости; в последнее время стало возможным исследование шейки бедренной кости. Основным недостатком метода является невозможность исследования осевого скелета.
Прогресс количественной компьютерной томографии привёл к развитию КТ с высокой разрешающей способностью. Возможно исследование как позвоночника (объёмная спиральная КТ), так и бедренной кости. Главной частью этих исследований является оценка трабекулярной структуры, или архитектоники [31]. Разрешающая способность в несколько десятков микрон позволяет рассчитывать стандартные гистоморфометрические параметры – объём трабекулярного вещества, число и ширину трабекул, пространство между ними [22]. Преимущество над гистоморфометрией, кроме неинвазивности, заключается в трёхмерной оценке трабекулярной структуры. Кроме того, проводится автоматический расчёт специфических показателей, отражающих качество соединения трабекул в единую сеть, имеющее прямое отношение к остеопорозу и прочности кости.
Одним из последних шагов в улучшении визуализации явилось внедрение компьютерной микротомографии (микро-КТ) [17]. С помощью основанной на принципе синхротронного излучения микро-КТ возможно достичь разрешающей способности менее 1 микрона, что позволяет в экспериментальных условиях визуализировать отдельные трабекулы, клетки костной ткани, оценивать пространственное распределение минералов и другие параметры [21].
УЛЬТРАЗВУКОВОЙ МЕТОД
Другим методом, предлагаемым для диагностики остеопороза и определения риска переломов, является количественное ультразвуковое исследование, часто неправильно называемое ультразвуковой денситометрией. Оно основано на взаимодействии звуковых (то есть механических) волн с костной тканью, близкой по своим свойствам к твёрдому телу, и в силу своей природы должно оценивать механические свойства кости. Методики КУИ являются параметрическими, результаты исследований представляются в виде количественной информации, связанной со свойствами кости: её массой и структурой [4]. В большинстве приборов определяется скорость ультразвука в костной ткани (в м/с), отражающая её плотность [42]. Скорость прохождения ультразвука является важной характеристикой биологических тканей и более объективно характеризует процесс распространения акустических волн по сравнению, например, с коэффициентом затухания [8]. Иногда (например, при исследовании пяточной кости) вычисляется и ослабление волны (в дБ/МГц), отражающее не только плотность ткани, но и состояние костных трабекул – их количество, пространственную ориентацию, наличие микроповреждений [5]. Скорость ультразвука и его затухание коррелируют между собой с коэффициентом 0,7, что предполагает воздействие на них разных свойств кости [19]. Если определяются оба параметра, то с помощью программного обеспечения в некоторых приборах они комбинируются в совокупный показатель (например, «жёсткость» [37]), что упрощает интерпретацию для клиницистов. Это делается и для достижения лучшей воспроизводимости, при этом, однако, может страдать диагностическая чувствительность методики. Наиболее часто исследуемые кости: пяточная [14], большеберцовая [12], фаланги пальцев [13, 43].
Применяется исследование и других костей, находящихся близко к поверхности тела: пястных, плюсневых, костей предплечья. Метод имеет ряд существенных недостатков, ограничивающих возможность его применения в практических условиях. Хотя для оценки результатов используются уже упоминавшиеся Т- и Z-критерии, не установлено значение Т-критерия, которое следует считать «пороговым»; за редким исключением исследуются только периферические кости; многие аппараты пропускают ультразвуковые волны только по кортикальному слою. Тем не менее, поскольку это исследование даёт информацию не только о содержании минералов, но и о других свойствах кости, определяющих её «качество» (прочность), метод может иметь определённые перспективы [38, 40].
РАДИОНУКЛИДНЫЙ МЕТОД
Радионуклидный (изотопный) метод ранее применялся достаточно широко. Использовались радиоизотопы гадолиния (153Gd) и йода (125I) соответственно для двухфотонной и однофотонной абсорбциометрии. Впоследствии их для генерации излучения заменили рентгеновской трубкой. Нейтронно-активационный анализ [34] в настоящее время редко используется для диагностики остеопороза ввиду его сложности. Его суть заключается в бомбардировке участков скелета нейтронами для получения нестабильного изотопа кальция (49Ca). Энергия, выделяющаяся при его распаде, отражает количество костных минералов.
Поиск новых методов изучения и диагностики остеопороза
Продолжается поиск новых методов изучения и диагностики остеопороза. Перспективным методом является магнитно-резонансная томография, сходная по своим возможностям с компьютерной томографией. При МРТ с высокой разрешающей способностью можно исследовать как осевой, так и практически любые участки периферического скелета [30, 32, 33]. Всё более широко в экспериментах используется магнитно-резонансная микротомография (микро- МРТ). Показано, что эта методика позволяет в опытах на животных фиксировать мельчайшие изменения костной архитектоники при развитии остеопороза, лекарственном воздействии и т. д. [15, 21].
Интересным аспектом микро-МРТ (как и микро-КТ) является возможность изучения состоятельности трабекулярной сети при её биомеханическом тестировании – динамическая микро-МРТ и микро-КТ [35]. Хотя есть сообщения об использовании методик со сверхвысокой разрешающей способностью в обследовании больных in vivo [26], основное применение такие методики нашли в доклинических условиях, что открыло новый этап изучения остеопороза и других метаболических заболеваний костной ткани.
С целью непосредственной оценки прочностных характеристик кости предпринимаются попытки определять её биомеханические свойства, в определённой степени моделируя устойчивость костей перед нагрузками. Механический анализ костной ткани использует низкочастотную вибрацию для получения ответа костной ткани, известного как «сгибательная жёсткость». Этот показатель является производным модуля эластичности Юнга и момента инерции и характеризует прочность кости. Наиболее часто для анализа используется локтевая кость [25]. В клинических условиях данный метод применения также пока не нашёл.
Таким образом, выбор метода исследования и оценка его результатов должны основываться на знании строения костной ткани, её физиологии, особенностей патогенеза конкретного варианта остеопороза и возможностей применяемых методов и методик. В клинических условиях непосредственно измерить костную массу и костную прочность пока невозможно. Поэтому в диагностике остеопороза используются показатели, оценивающие их косвенно. В настоящее время наилучшей методикой, опосредованно оценивающей костную массу, считается двухэнергетическая рентгеновская абсорбциометрия, измеряющая минеральную плотность костной ткани.
Другим направлением в развитии диагностических средств при остеопорозе является изучение и оценка костной микроструктуры. Необходимость её изучения вытекает из того важного в практическом отношении факта, что на риск остеопоротических переломов микроархитектоника и костная масса оказывают независимое друг от друга влияние. В этой связи наиболее перспективным является сочетание обоих подходов в исследовании костной ткани при остеопорозе.
Р. Е. Чечурин. Январь 2001.
СПИСОК ЛИТЕРАТУРЫ
- Baran D. T., Faulkner K. G., Genant H. K., Miller P. D., Pacifici R. Диагностика и лечение остеопороза: принципы использования костной денситометрии // Остеопороз и остеопатии. – 1998. – № 3. – С. 10 – 16.
- Белосельский Н. Н. Рентгеновская морфометрия позвоночника в диагностике остеопороза // Остеопороз и остеопатии. – 2000. – № 1. – С. 23 – 26.
- Власова И. С. Компьютерная томография в диагностике остеопороза // Остеопороз и остеопатии. – 1998. – № 2. – С. 13 – 15.
- Gluer C. C. Роль количественной ультразвуковой денситометрии в диагностике остеопороза // Остеопороз и остеопатии. – 1999. – № 3. – С. 33 – 39.
- Дамбахер М. А., Шахт Е. Остеопороз и активные метаболиты витамина D: англ. – Basle, Switzerland: Eular Publishers, 1996. – 140 с.
- Оценка риска переломов и её применение для скрининга постменопаузального остеопороза. Доклад Рабочей группы ВОЗ. – Женева: Всемирная организация здравоохранения, 1994. – 184 с.
- Поляков В. А., Чемянов Г. Г. Искусственная синтетическая костная ткань. – Москва: Издательство Российской медицинской академии последипломного образования, 1996. – 70 с.
- Применение ультразвука в медицине. Физические основы: англ. / Под ред. К. Хилла. – Москва: Мир, 1989. – 568 с.
- Рожинская Л. Я. Системный остеопороз. Москва: КРОН-ПРЕСС, 1996. – 208 с.
- Чечурин Р. Е., Аметов А. С., Рубин М. П. Сравнительная оценка рентгеновской денситометрии осевого скелета и ультразвуковой денситометрии пяточной кости // Остеопороз и остеопатии. – 1999. – № 4. – С. 7 – 10.
- Andresen R., Haidekker M. A., Radmer S., Banzer D. CT determination of bone mineral density and structural investigations on the axial skeleton for estimating the osteoporosis-related fracture risk by means of a risk score // Br. J. Radiol. – 1999. – V. 72. – № 858. – P. 569 – 578.
- Augat P., Fan B., Lane N. E., Lang T. F., LeHir P., Lu Y., Uffmann M., Genant H. K. Assessment of bone mineral at appendicular sites in females with fractures of the proximal femur // Bone. – 1998. – № 22. – Р. 395 – 402.
- Benitez C. L., Schneider D. L., Barrett-Connor E., Sartoris D. J. Hand ultrasound for osteoporosis screening in postmenopausal women // Osteoporos. Int. – 2000. – V. 11. – № 3. – P. 203 – 210.
- Bone ultrasonometry: is it equal or superior to DEXA? // Lunar News. – 2000; Winter. – Р. 3 – 6.
- Borah B., Dufresne T. E., Cockman M. D., Gross G. J., Sod E. W., Myers W. R., Combs K. S., Higgins R. E., Pierce S. A., Stevens M. L. Evaluation of changes in trabecular bone architecture and mechanical properties of minipig vertebrae by three- dimensional magnetic resonance microimaging and finite element modeling // J. Bone Miner. Res. – 2000. – V. 15. – № 9. – P. 1786 – 1797.
- Consensus development conference: diagnosis, prophylaxis and treatment of osteoporosis // Am. J. Med. – 1993. – № 94. – Р. 646 – 650.
- Engelke K., Karolczak M., Seibert U., Lutz A., Kalender W. A. Micro-CT at 10 micron spatial resolution // Osteoporos. Int. – 2000. – V. 11. – Suppl. 3. – P. S9.
- Frost H. M. Perspective: changing views about 'osteoporoses' (a 1998 overview) // Osteoporos. Int. – 1999. – V. 10. – № 5. – P. 345 – 352.
- Genant H. K., Guglielmi G., Jergas M. (eds.). Bone Densitometry and Osteoporosis. – Springer, 1998. – 604 p.
- Grampp S., Henk C. B., Imhof H. CT and MR assessment of osteoporosis // Semin. Ultrasound CT MR. – 1999. – V. 20. – № 1. – P. 2 – 9.
- Gross G. J., Dufresne T. E., Smith T., Cockman M. D., Chmielewski P. A., Combs K. S., Borah B. Bone architecture and image synthesis // Morphologie. – 1999. – V. 83. – № 261. – P. 21 – 24.
- Haidekker M. A., Andresen R., Werner H. J. Relationship between structural parameters, bone mineral density and fracture load in lumbar vertebrae, based on high- resolution computed tomography, quantitative computed tomography and compression tests // Osteoporos. Int. – 1999. – V. 9. – № 5. – P. 433 – 440.
- Horikoshi T., Endo N., Uchiyama T., Tanizawa T., Takahashi H. E. Peripheral quantitative computed tomography of the femoral neck in 60 Japanese women // Calcif. Tissue Int. – 1999. – V. 65. – № 6. – P. 447 – 453.
- Jergas M., Schmid G. Conventional radiology of osteoporosis and radiographic absorptiometry // Radiologe. – 1999. – V. 39. – № 3. – P. 174 – 185.
- Kiebzak G. M., Box J. H., Box P. Decreased ulnar bending stiffness in osteoporotic caucasian women // J. Clin. Densitom. – 1999. – V. 2. – № 2. – P. 143 – 152.
- Kohlbrenner A., Ruegsegger P. Multiple fan beam microtomography for in- vivo examinations of humans and laboratory animals // Osteoporos. Int. – 2000. – V. 11. – Suppl. 3. – P. S9.
- Krane St. M. Assessment of mineral and matrix turnover. In: Frame B., Potts J. T. Jr. (eds.). Clinical disorders of bone and mineral metabolism. – Excerpta medica. Internat. Congress Series 617. Amsterdam, Oxford, Princeton. – 1983. – P. 95 – 98.
- Lang T., Augat P., Majumdar S., Ouyang X., Genant H. K. Noninvasive assessment of bone density and structure using computed tomography and magnetic resonance // Bone. – 1998. – V. 22. – № 5 (Suppl.). – P. 149S – 153S.
- LeGeros R. Z. Biological and synthetic apatites. In: Brown P. W., Constantz B. (eds.). Hydroxyapatite and related materials. – CRC, Boca Raton, 1994. – P. 3 – 28.
- Link T. M., Majumdar S., Augat P., Lin J. C., Newitt D., Lu Y., Lane N. E., Genant H. K. In vivo high resolution MRI of the calcaneus: differences in trabecular structure in osteoporosis patients // J. Bone Miner. Res. – 1998. – V. 13. – № 7. – P. 1175 – 1182.
- Link T. M., Majumdar S., Grampp S., Guglielmi G., van Kuijk C., Imhof H., Gluer C., Adams J. E. Imaging of trabecular bone structure in osteoporosis // Eur. Radiol. – 1999. – V. 9. – № 9. – P. 1781 – 1788.
- Majumdar S., Genant H. K. High resolution magnetic resonance imaging of trabecular structure // Eur. Radiol. – 1997. – V. 7. – Suppl. 2. – P. S51 – S55.
- Majumdar S. A review of magnetic resonance (MR) imaging of trabecular bone micro-architecture: contribution to the prediction of biomechanical properties and fracture prevalence // Technol. Health Care. – 1998. – V. 6. – № 5. – P. 321 – 327.
- Muller C. G., Harrison J. E., Sturtridge W. C., Becker E. J., Lui S., Strauss A., Goodwin S. Relative sensitivities of dual-energy X-ray absorptiometry and in vivo neutron activation analysis for the diagnosis of osteoporosis // Basic Life Sci. – 1993. – № 60. – P. 45 – 48.
- Muller R., Gerber S. C., Hayes W. C. Micro-compression: a novel technique for the nondestructive assessment of local bone failure // Technol. Health Care. – 1998. – V. 6. – № 5. – P. 433 – 444.
- Peck W. A., Burckbardt P., Christiansen C. et al. Consensus development conference: diagnosis, prophylaxis, and treatment of osteoporosis // Am. J. Med. – 1993. – № 94. – P. 646 – 650.
- Pluskiewicz W., Drozdzowska B. Ultrasound measurements at the calcaneus in men: differences between healthy and fractured persons and the influence of age and anthropometric features on ultrasound parameters // Osteoporos. Int. – 1999. – № 10. – Р. 47 – 51.
- Schott A. M., Weill-Engerer S., Hans D., Duboeuf F., Delmas P. D., Meunier P. J. Ultrasound discriminates patients with hip fracture equally well as dual energy x-ray absorptiometry and independently of bone mineral density // J. Bone Miner. Res. – 1995. – № 10. – Р. 243 – 249.
- Smith J., Shoukri K. Diagnosis of osteoporosis // Clin. Cornerstone. – 2000. – V. 2. – № 6. – P. 22 – 33.
- Turner C. H., Peacock M., Schaefer C. A., Timmermann L., Johnston C. C. Jr. Ultrasonic measurements discriminate hip fractures independently of bone mass // J. Bone Miner. Res. – 1994. – № 9 (suppl. 1). – Р. S157.
- Van Rietbergen B., Majumdar S., Pistoia W., Newitt D. C., Kothari M., Laib A., Ruegsegger P. Assessment of cancellous bone mechanical properties from micro-FE models based on micro-CT, pQCT and MR images // Technol. Health Care. – 1998. – V. 6. – № 5. – P. 413 – 420.
- Walsh W. R., Labrador D. P., Kim H. D., Guzelsu N. Annals of Biomedical Engineering. – 1994. – № 22. – Р. 404 – 415.
- Wuster C., Albanese C., De Aloysio D., Duboeuf F., Gambacciani M., Gonnelli S., Gluer C. C., Hans D., Joly J., Reginster J. Y., De Terlizzi F., Cadossi R. Phalangeal osteosonogrammetry study: age-related changes, diagnostic sensitivity, and discrimination power. The Phalangeal Osteosonogrammetry Study Group // J. Bone Miner. Res. – 2000. – V. 15. – № 8. – P. 1603 – 1614.